
透射电镜(Transmission Electron Microscope,TEM),全称透射电子显微镜,是把经加速和聚集的电子束投射到超薄切片的样品上(通常70-90nm),电子与样品中的原子碰撞而改变方向,从而产生立体角散射。散射角的大小与样品的密度、厚度相关,因此可以形成明暗不同的影像,影像将在放大、聚焦后在成像器件上显示出来。是一种高分辨率(0.1nm-0.2nm)、高放大倍数(0.2K-600K)的显微镜。是观察和研究物质超微结构的强有力工具。
透射电镜在细胞生物学、组织学、病毒学、病理学、分子生物学、材料科学等诸多领域具有广泛应用。可以观测动物植物细胞超微结构,如线粒体、内质网、高尔基体、溶酶体、叶绿体、液泡、细胞内生细菌等结构及病理变化。可以观测病毒颗粒、外泌体、病原微生物、各类细菌真菌、纳米材料及纳米颗粒、晶体结构。
1、平台主要设备:超薄切片机Leica EM UC7,透射电镜HITACHI HT7800 120kV。
HT7800系列产品的最大特点是采用日立最新设计的第二代双隙物镜,很好地继承了日立120kV-TEM的基本理念,兼顾低倍率与宽视野观察、高衬度与高分辨率观察,可在同一仪器上一键切换等。集高衬度和高分辨两种模式于一体,可同时满足软材料/纳米材料类和生命科学类客户对电镜的需求。
HT7800使用高速高灵敏度的CMOS荧光屏相机取代了传统的荧光屏观察窗,将 TEM 操作统一于显示器上,实现透射电镜操作的全数字化,可以在明亮的室内进行观察。这样,既可以保护操作者和样品,也可以显著改善操作环境。
2、透射电镜HITACHI HT7800主要技术指标:
(1)分辨率(晶格):0.2nm(120kV,off-axis)。
(2)放大倍数:(HC模式) ×200~×200,000;(HR模式) ×4,000~×600,000;(低倍模式) ×50~×1,000
由电子枪发射出来的电子束,在真空通道中沿着镜体光轴穿越聚光镜,通过聚光镜将之汇聚成一束尖细、明亮而又均匀的光斑,照射在样品室内的样品上里透过样品后的电子束携带有样品内部的结构信息,样品内致密处透过的电子量少,稀疏处透过的电子量多;经过物镜的会聚调焦和初级放大后,电子束进入下级的中间透镜和第1、第2投影镜进行综合放大成像,最终被放大了的电子影像投射在观察室内的荧光屏上;荧光屏将电子影像转化为可见光影像以供使用者观察。
1、接收样本。
2、核对编号,沟通切面以及拍照要求。
3、电镜制样。
4、镜下预览观察样本。
5、正式实验拍照。
科研样本透射电镜取材
注*由于每个人操作习惯以及所用试剂会有差别,以下操作仅供参考
一.实验前准备
1. 检索文献,充分检索文献,明确是否需要做超微结构,是否有光镜的研究基础,适合采用何种EM技术,实验设计以及预期结果
2. 设计取材方案,明确器官、部位、方向、大小,多少,解剖定位的方式等等
3. 实验材料,根据取材设计方案做好准备,动物,器材,试剂等等
4. 沟通与配合,实验室与课题组双方对研究内容和有关的技术问题充分沟通。
二.组织取材
1.取材的准备工作:
提前查询文献资料,确定取材方法、取材部位、组织切面等。
所需器械均需实验室温度一致即可:镊子、双面刀片(用于切割、细修生物样品),放有2.5%戊二醛固定液的EP小管若干(必须干净),冰盒一个,蜡板/塑料平皿,牙签及吸管多根,生理盐水等。
2.取材方法:
将动物麻醉,暴露待取脏器,在不中断血液供应的情况下用锋利刀片切下一小块目标组织及时放入固定液中,洁净蜡板上滴入足够固定液形成液滴,使组织能充分浸没固定液,组织迅速放入洁净蜡板固定液中,用新的双面刀片将组织修小(1mm3,或1x1x2mm3长条状),用牙签将修好的组织小块轻轻挑入装有常温戊二醛固定液的EP小管(事先贴好标签)内浸泡固定15-30min,不可用力夹取,密封,置于4℃冰箱内保存。注:组织离开活体后,要求在0.5~2分钟内完成修块到浸入醛类固定液的操作过程。
如果组织块带有较多血液或组织液,用滴管吸取常温缓冲液(0.1M PBS)或等渗生理盐水(0.9%NS)把血液和组织液冲掉,迅速放入蜡板上的固定液小滴中细修成小块。
原位固定:保持器官血液供应情况下,边解剖边将固定液(常温)滴加到取材部位,减少组织自溶,使组织达到适当硬度后切取,即刻将组织置入固定液中,
灌注固定:对于脑组织和脊髓可以推荐灌注固定,不同实验室环境温度不同,季节不同,灌注过程需要注意温度影响;灌注压的精准控制几乎无法实现,灌注固定会引起“人工假象”,比如观察血脑屏障、肝窦;如果灌注条件不成熟或者灌注不熟练,建议快速取材固定。
3.组织取材要点:
(1)定位准确:取材部位准确。肾脏、胰岛、脑等不同部位有不同组织结构,应根据研究目的和要求确定切取部位,对照组与实验组的取材组织区位、方向,应严格一致并有代表性。
(2)操作迅速:离开活体后的组织应快捷地(<2min)浸入固定液(事先准备好醛类固定液置2ml圆底离心管,常温),直接快捷地取材。
(3)样品尺寸厚度:组织块厚度首先要与固定液渗透率(≤0.5mm)相适应,样品块过大,内部固定不良。将较大的组织块修切成符合要求的TEM标本时,须事先备好蜡板/干净平皿,滴上固定液,快速将样品浸在液滴中修切,确认修切的样品条均包含目标结构,组织厚度≤2mm(厚度最好≤1mm),用牙签挑出3-4条,置入电镜固定液(室温/4℃)中,即刻密闭。
(4)操作轻柔、清洁:取材操作动作始终保持轻柔,尽可能避免金属器具对组织的夹持、挤压或牵拉,严禁用剪刀剪取组织,所用器具必须清洁,使用缓冲液清洗。
(5)使用合适的温度:灌注固定液、缓冲液,灌注均采用室温(25℃左右)/接近生理温度;较高温度(如室温25℃左右)可以提高固定液渗透效率,但增加温度会导致组织自溶;反之,低温(如4℃)可以减缓细胞自溶,但会降低固定液渗透速率,两者应兼顾;一般刚解剖切取的组织块浸入常温醛类固定液,然后再将组织按照电镜取材大小要求进行取材切取,继续进行固定,采用常温固定15-30min后,样本再放置4℃保存;如果初始固定液体温度是4℃,建议常温固定1-2小时后,样本再放置4℃保存。
(6)固定液体积:样本4℃保存,建议固定液体积是样本体积10-20倍以上。

三. 取材形状和方向性
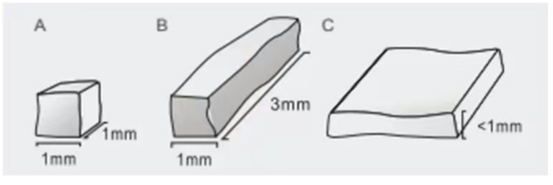
1). 例图1
A:正方体形态样本颗粒:约1mm×1mm×1mm。
B:长方体样本条:约1mm×1mm×3mm。
C:薄片状样本:约1mm×2mm×3mm。
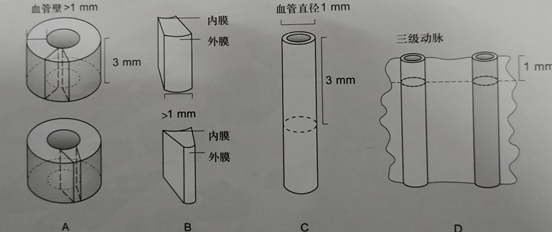
2). 例图2
A、B:血管管壁厚度大于1mm血管
C:血管直径小于等于1mm
D:小动脉取材
四. 不同组织类型取材建议
1)韧带、皮肤、骨骼肌等有方向性组织:根据组织方向,修成长条状/片状,皮肤需要剔除毛发(不要拔除毛发),骨骼肌取材采用灌注固定方法可以参考文献。
取材例图

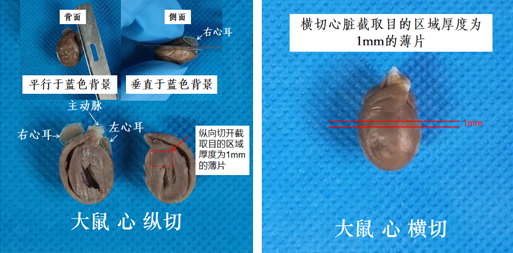
2)心肌组织:
固定方法推荐:及时取材固定,沿着主动脉到心尖方向,切开暴露整个心脏解剖切面,然后再将组织按照电镜取材大小要求进行取材,继续进行固定。
如果观察冠状动脉,可以考虑横切心脏组织
取材例图
3)肠道、气管等空腔性组织:根据管腔厚度切成一定具有方向性形状,也可以纵向切开腔面。
取材例图

4)血管:注意组织直径和方向性。
取材例图

5)肺组织,组织中有气体影响固定效果,可以采取气管、主动脉灌流、或者心脏灌注固定方法(灌注会造成肺组织肿胀形变,不利于观察肺泡中巨噬细胞),灌注固定后再取材目的区域,组织切取厚度小于1mm;如果没有灌注固定,及时切取组织后尽快固定,为了减少组织漂浮因素造成的影响,可以抽真空使其完全沉到瓶底为止,或用小纱布包裹后将组织浸没到固定液中,使组织能得到充分浸没在固定液中,如果关注重点是支气管,需要注意取材区域以及方向。
取材例图

6)眼球(视网膜、脉络膜、巩膜结构)
固定方法推荐:1、快速取出眼球,眼球放入固定液中,2、在蜡板上滴加固定液,组织置于固定液中,组织正中将角膜用锋利刀片划开半周,房水流出,3、眼球置于固定液中,常温固定30-60min后,换新的电镜固定液,样本置于4℃保存,固定液体积是组织体积10倍以上,
如果眼球比较大:快速取出眼球,及时投入固定液,用注射器从角膜回抽后向眼内注射固定液快速固定,眼球投入固定液中固定10-15min后,组织正中将角膜用锋利刀片划开半周,眼球置于固定液中,常温固定30-60min后,换新的电镜固定液,样本置于4℃保存,固定液体积是组织体积10倍以上,
取材大小和形状:

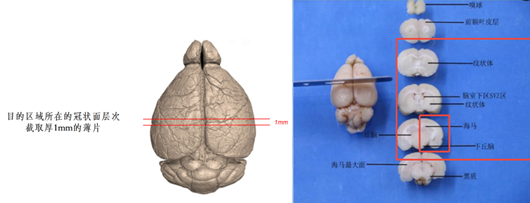
7)髓鞘、脑组织:
脑组织结构复杂,脑组织注意部位定位,可以先进行灌注固定,然后取材整个脑组织,按照冠状面方向切开脑组织形成1mm薄片,再根据实验目的区域切取相应部位,做定向包埋;固定温度如果关注重点是神经髓鞘(胼胝体)结构,建议是常温固定2小时,然后样本置于4℃保存,固定液体积是组织体积10-20倍以上,
8)肝脏、胰腺(胰岛取材胰尾部分)

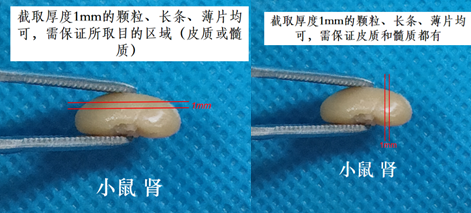
9)肾脏(肾小球区域取材皮质)
取材例图
10)睾丸
固定方法推荐:组织比较松散,根据组织大小,如果是观察生精小管,可以采用原位固定、及时取材固定;
对于体积比较大的睾丸组织取材,睾丸组织及时投入固定液,用注射器插入睾丸内部,从多个方向注射固定液,组织浸泡在固定液中常温固定10-15min,然后再将组织按照电镜取材大小要求进行取材,继续进行固定。
取材示例

11)毛发
取材大小和形状:包含完整毛囊

12) 骨头组织
取材大小和形状:厚度1mm左右,大小约1mm×1mm×3mm;约1mm×2mm×3mm。
固定后需要进行脱钙,脱钙后才能进行后续样本处理流程。
13)脂肪组织
及时取材,固定的脂肪组织尽可能小一些,正方体形态样本颗粒:约1mm×1mm×1mm,脂肪不易被醛类固定,建议短时间内制样
五.培养细胞取材
保证细胞活性状态的情况下,尽快固定,如果要观察凋亡、焦亡、死亡等现象,需要收集干预后漂浮的细胞、贴壁比较松的细胞。
凋亡、焦亡、死亡等的发生有一个最佳检测时间窗,宏观上有时很难找准。因此除非已有经验或进行了充分的预试,最好不要在筛查和大规模实验中,将电镜观察作为首选方法。

1.贴壁细胞
对于单层贴壁细胞的透射电镜观察制样方法主要由三种:消化离心法、刮除离心法、原位包埋法。
1.1 消化离心法(消化时间控制在1min以内;短时离心收集,如果细胞消化时间较长,或难消化,不推荐此方法,)
1)确认细胞数量充足,需要用到6-10cm平皿/6孔板1-2个孔,细胞数量大约5×105-106,具体根据对应的细胞大小、生长密度而定;离心后细胞团约1个芝麻-绿豆粒大小。
2)常规胰酶消化细胞,用完全培养基终止消化,离心收集细胞悬液。把细胞悬液置入洁净 1.5ml 尖头 EP 管内。
3)转速2000-3000rpm 离心 2min-3min(根据实际情况适当增减速度),弃去上清,离心后在 ep 管底细胞沉淀成团(细胞团约1个芝麻-绿豆粒大小)。
4)弃去上清,留取致密细胞团,缓慢注入1-2ml 常温 2.5%戊二醛固定液,混匀细胞,EP管内灌满固定液,室温避光固定3-5min,转入4℃保存。
1.2 刮除离心法
1)确认细胞数量充足,需要用到6-10cm平皿/6孔板1-2个孔,不建议用培养瓶,细胞数量大约5×105-106,具体根据对应的细胞大小、生长密度而定;离心后细胞团约1个芝麻-绿豆粒大小。
2)弃去培养液后,迅速加足量常温 2.5%戊二醛固定3-5min(戊二醛完全浸没细胞)。
3)随后用细胞铲或细胞刮成 45°倾角轻柔刮下细胞。顺着一个方向,不要来回刮细胞。
4)将细胞悬液全部转移到1.5ml 尖头 EP 管内。
5)转速1000-2000rpm 离心 5min-10min(根据实际情况适当增减),弃去上清。
6)细胞沉淀成团(细胞团约1个芝麻-绿豆粒大小)注入1-2ml 常温 2.5%戊二醛固定液,用牙签挑起(也可以混匀),使细胞沉淀不要沉底,EP管内灌满固定液,转入4℃保存。
注意:请客户明确观察的目的,选择合适的固定方法
1.消化离心法最简单易行,但是消化后细胞的形状结构不是培养状态下,对于消化不敏感的细胞(消化时间长),不建议用此方法。
2、刮除离心法细胞更加接近于培养状态,如果是实验设计中短时间内的干预和刺激细胞,可以选择用刮除离心法,此方法会机械损伤细胞。
4. 悬浮细胞(离心条件根据实际情况调整)
将细胞悬液全部转移到1.5ml 尖头 EP 管(或者15ml尖底离心管)内,转速1000-2000rpm 离心5-10min成团(细胞团约1个芝麻-绿豆粒大小),轻轻吸去上清液(切勿丢失细胞),再沿管壁缓缓加入 1ml 常温 2.5%戊二醛,混匀细胞,EP管内灌满固定液,室温避光固定3-5min,转入4℃保存。
5. 关于细胞量以及混匀的建议
1)收集细胞数量需要适量,细胞团约1个芝麻-绿豆粒大小,如果细胞沉淀比较大(绿豆、黄豆大小),需要考虑多加入固定液(大于2ml),固定液体积不能太少,固定液充分。
2) 固定方法决定,消化后离心收集细胞沉淀,如果沉淀比较小(1mm厚度),可以挑起沉淀,如果沉淀比较大,最好是挑散或者混匀,主要考虑固定液及时充分固定效率;同样的如果是固定后刮下来收集细胞,也要考虑沉淀大小。
六.细菌:吸取OD0.5-0.8(保持细菌培养活力的前提下)的培养物至1.5mL离心管中,一般7000 rpm离心5min(根据实际情况调整),菌体沉淀于管底,沉淀体积需要芝麻-绿豆粒大小,弃掉上清液,加满室温2.5%的戊二醛固定液,移液器吹散混匀沉淀,室温放置半小时后转入4℃冰箱中保存
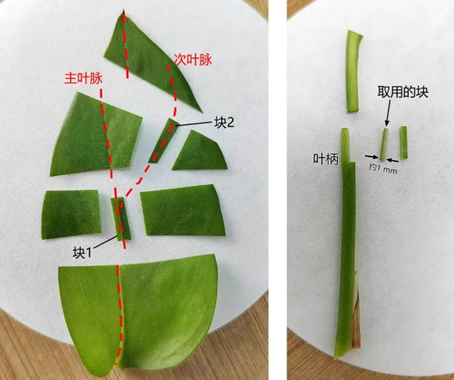
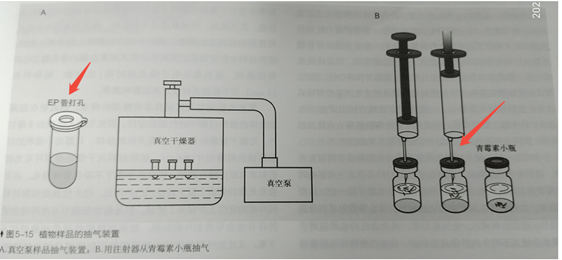
八.植物材料的获取:叶片组织取1×1×3㎜长条;根、茎果实切取1mm3小块;建议所有叶片组织均需抽真空,使样品沉入固定液中,也可以用4%戊二醛固定1-2h,再换2.5%戊二醛
真空示意图:



 关注百奥斯公众号
关注百奥斯公众号
 打开百奥斯小程序
打开百奥斯小程序